Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
池部 仁善; 河野 秀俊
no journal, ,
ヌクレオソームのヒストンテイル領域は、クロマチン構造の形成や、ヒストンテイルへの官能基修飾によってDNA機能が制御されるヒストンコード仮説などに深くかかわっていることが知られており、生物学的に重要である。これらの現象のメカニズムを解明するには、ヌクレオソームコア粒子(Nucleosome Core Particle: NCP)と違って特定の安定構造を持たないと考えられる、ヒストンテイルの動態を詳細に調べる必要がある。分子動力学シミュレーションは、このような構造的揺らぎの大きい生体分子の構造変化を原子レベルで解析できる優れた手法であるが、従来の手法では計算資源の問題等から、ヌクレオソームから切り離されたヒストンテイル断片のシミュレーション研究しか行われていなかった。そこで本研究では、われわれが新たに開発した、高い効率でヒストンテイルの安定構造を探索できるadaptive 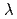 dynamicsという手法を用いて、ヒストンテイル周辺のNCPと溶媒水分子をあらわに計算に取り入れたシミュレーションを行う。本発表では、本計算の途中経過について発表する。
dynamicsという手法を用いて、ヒストンテイル周辺のNCPと溶媒水分子をあらわに計算に取り入れたシミュレーションを行う。本発表では、本計算の途中経過について発表する。
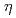 の損傷乗り越え修復メカニズムの理解に向けて
の損傷乗り越え修復メカニズムの理解に向けて石田 恒
no journal, ,
DNAポリメラーゼ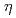 は、紫外線損傷のひとつであるチミン二量体を乗り越えてDNA合成反応を行うことのできるDNAポリメラーゼである。2010年に解かれたヒトDNAポリメラーゼ
は、紫外線損傷のひとつであるチミン二量体を乗り越えてDNA合成反応を行うことのできるDNAポリメラーゼである。2010年に解かれたヒトDNAポリメラーゼ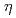 (Pol
(Pol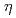 )と シクロブタン型ピリミジン2量体(CPD)を含むDNAの複合体のX線結晶構造から、Pol
)と シクロブタン型ピリミジン2量体(CPD)を含むDNAの複合体のX線結晶構造から、Pol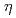 のCPD認識に関する理解が多いに進んだ。しかしながら、Pol
のCPD認識に関する理解が多いに進んだ。しかしながら、Pol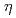 が損傷部位であるCPDをどのように乗り越え、かつ同時にDNA複製を行うのかを理解するには、Pol
が損傷部位であるCPDをどのように乗り越え、かつ同時にDNA複製を行うのかを理解するには、Pol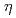 とDNAの静的な立体構造における相互作用のみならず動的メカニズム(Pol
とDNAの静的な立体構造における相互作用のみならず動的メカニズム(Pol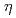 のドメイン運動、CPD認識部位の原子運動など)についての理解が必要である。Pol
のドメイン運動、CPD認識部位の原子運動など)についての理解が必要である。Pol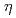 の損傷乗り越え複製機構の動的メカニズムを理解するために、Pol
の損傷乗り越え複製機構の動的メカニズムを理解するために、Pol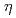 がCPDを乗り越えてDNA上を移動する過程を分子動力学シミュレーションを用いて観測することを試み始めた。初めの試みとして、Pol
がCPDを乗り越えてDNA上を移動する過程を分子動力学シミュレーションを用いて観測することを試み始めた。初めの試みとして、Pol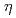 とCPDのX線結晶構造において、CPDを正常チミンに置換する自由エネルギー摂動法を実施し、Pol
とCPDのX線結晶構造において、CPDを正常チミンに置換する自由エネルギー摂動法を実施し、Pol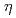 のCPDに対する結合能を解析した。本研究会では、Pol
のCPDに対する結合能を解析した。本研究会では、Pol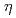 のCPD認識解析、及びPol
のCPD認識解析、及びPol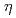 のDNA上移動過程を調べるための方法について発表する。
のDNA上移動過程を調べるための方法について発表する。